職位推薦
- 珍格醫(yī)療-臨床銷售 15001-20000
- 地奧制藥-醫(yī)藥代表 6001-8000
- 普利德醫(yī)療-醫(yī)療設(shè)備銷售經(jīng)理 面議
- 大唐-兼職招商經(jīng)理 面議
- 景德中藥-直營(yíng)經(jīng)理 6001-8000
- 安邦醫(yī)藥-省區(qū)招商經(jīng)理 8001-10000
- 恒瑞醫(yī)藥-醫(yī)藥信息溝通專員 6001-8000
- 黃河中藥-學(xué)術(shù)講師 8001-10000

發(fā)布日期:2025-10-14 瀏覽次數(shù):52
近日,我院超聲醫(yī)學(xué)科邱邐教授團(tuán)隊(duì)在Signal Transduction and Targeted Therapy(STTT,IF:52.7)發(fā)表題為“Ultrasound-enhanced Pt-coordinated polymer immunopotentiators and heterogenic fusion membrane-based multifunctional tumor vaccine nanoplatforms for melanoma treatment” 的研究文章。該研究構(gòu)建了一種基于金黃色葡萄球菌胞外囊泡(EVs)與黑色素瘤細(xì)胞膜(CM)的異源融合膜腫瘤疫苗EV-CM,并進(jìn)一步整合Pt-卟啉配位聚合物免疫增強(qiáng)劑(CPIP),形成了CPIP@EV-CM多功能納米疫苗平臺(tái)。該平臺(tái)聯(lián)合聲動(dòng)力治療(SDT)及化學(xué)動(dòng)力治療(CDT),能夠有效激活抗腫瘤免疫應(yīng)答,預(yù)防腫瘤的發(fā)生、清除原位腫瘤并抑制遠(yuǎn)處轉(zhuǎn)移,為黑色素瘤的免疫治療提供了一個(gè)新思路。

超聲醫(yī)學(xué)科馬朗研究員、邱邐教授為共同通訊作者,郭瑞倩、杜方雪博士后為共同第一作者。我院為第一作者單位。該工作得到了國(guó)家自然科學(xué)基金、中國(guó)博士后科學(xué)基金、四川省科技廳等項(xiàng)目資助。
腫瘤免疫治療已成為繼手術(shù)、化療和放療后的有效治療手段。通過實(shí)現(xiàn)靶向遞送、抗原呈遞和免疫激活,基于腫瘤細(xì)胞膜(CM)的仿生納米平臺(tái)已成為一種新興的腫瘤防治策略。腫瘤細(xì)胞膜富含包括個(gè)性化新抗原在內(nèi)的多種抗原,可被抗原呈遞細(xì)胞(APCs)識(shí)別并攝取,進(jìn)而激活下游抗腫瘤免疫應(yīng)答。然而,單一腫瘤細(xì)胞膜的免疫原性較低,阻礙了APCs的有效激活。融合膜仿生策略通過融合均質(zhì)細(xì)胞或膜組分來(lái)實(shí)現(xiàn)腫瘤抗原與免疫刺激劑的協(xié)同遞送,這一創(chuàng)新方法為構(gòu)建腫瘤疫苗開辟了新途徑。此外,通過在融合膜內(nèi)部裝載不同應(yīng)用模塊(治療/成像/載藥等),可靈活滿足不同設(shè)計(jì)需求,形成多功能腫瘤納米疫苗平臺(tái)。
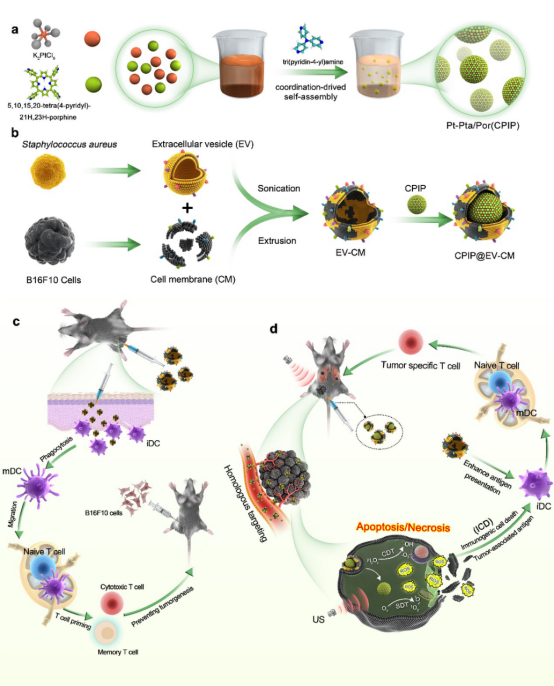
圖1. CPIP@EV-CM納米疫苗的構(gòu)建及其用于增強(qiáng)腫瘤免疫治療的示意圖
細(xì)菌胞外囊泡(EV)是由細(xì)菌自發(fā)形成膜囊泡,因其以非復(fù)制形式繼承了母體細(xì)菌的天然佐劑標(biāo)記,被視為理想的免疫刺激劑。研究團(tuán)隊(duì)將B16F10黑色素瘤細(xì)胞膜與金黃色葡萄球菌來(lái)源的胞外囊泡膜融合,成功制備了EV-CM異源融合膜。該融合膜繼承了親本組分的抗原性和佐劑標(biāo)志物,能夠在體外高效激活樹突狀細(xì)胞(DCs)。在小鼠足墊皮下注射EV-CM融合膜后,其能快速遷移至局部引流淋巴結(jié),實(shí)現(xiàn)腫瘤抗原的高效遞送。
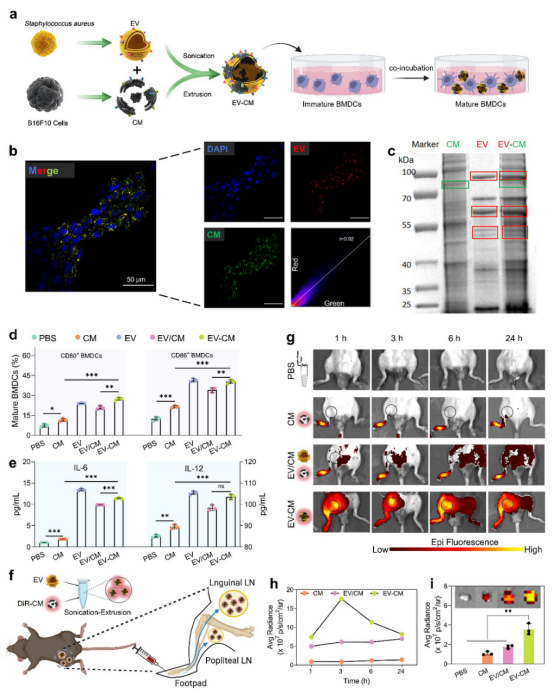
圖2. EV-CM融合膜的表征及其免疫激活潛能評(píng)估
體內(nèi)腫瘤預(yù)防實(shí)驗(yàn)表明,皮下免疫后接種腫瘤細(xì)胞,EV-CM融合膜疫苗能顯著抑制黑色素瘤的發(fā)生;與單純腫瘤細(xì)胞膜免疫組相比,小鼠的無(wú)瘤生存時(shí)間從14天延長(zhǎng)至19天。EV-CM免疫組CD8+T細(xì)胞及活化的CD8+T細(xì)胞(CD69+CD8+T)比例明顯增加,且效應(yīng)記憶T細(xì)胞比例顯著升高,揭示了腫瘤預(yù)防作用的潛在機(jī)制。
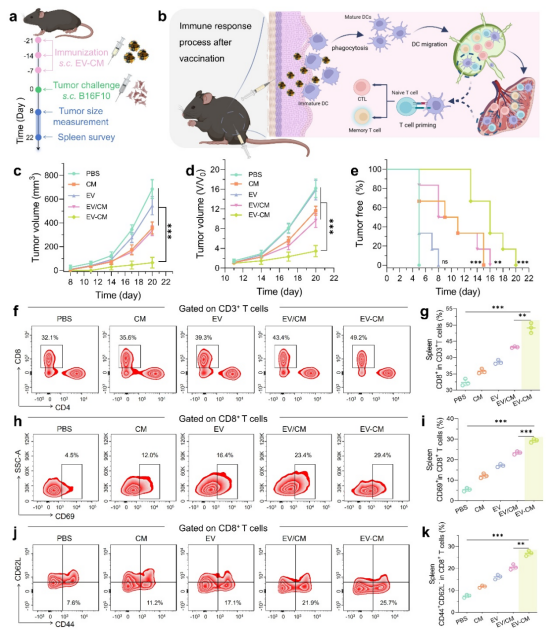
圖3. 小鼠黑色素瘤預(yù)防效果評(píng)估
為進(jìn)一步提高對(duì)已發(fā)生腫瘤的清除能力,研究團(tuán)隊(duì)將聲動(dòng)力/化學(xué)動(dòng)力治療模塊——Pt-卟啉配位聚合物免疫增強(qiáng)劑(CPIP)裝載于EV-CM融合膜,構(gòu)建出具有核殼結(jié)構(gòu)的多功能納米疫苗CPIP@EV-CM。體外實(shí)驗(yàn)表明,在超聲輻照下,CPIP@EV-CM能高效產(chǎn)生活性氧(ROS)直接殺傷腫瘤細(xì)胞。
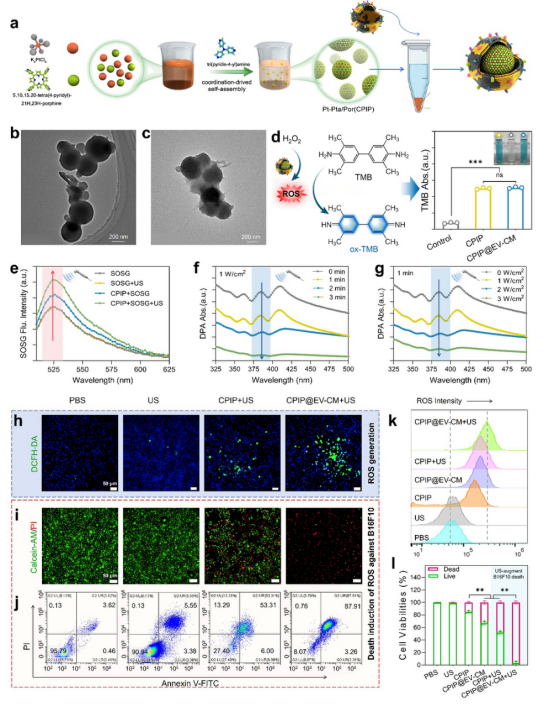
圖4. CPIP@EV-CM的制備、表征及其體外直接腫瘤殺傷效果評(píng)估
此外,聲動(dòng)力/化學(xué)動(dòng)力治療能夠有效誘導(dǎo)腫瘤細(xì)胞發(fā)生免疫原性細(xì)胞死亡(ICD),促進(jìn)DCs成熟和促炎細(xì)胞因子分泌,進(jìn)一步增強(qiáng)免疫治療效果。
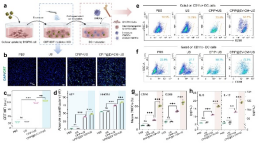
圖5. CPIP@EV-CM介導(dǎo)的體外ICD效應(yīng)和免疫刺激反應(yīng)
體內(nèi)治療結(jié)果顯示,CPIP@EV-CM聯(lián)合超聲輻照能有效抑制小鼠黑色素瘤生長(zhǎng),抑瘤率達(dá)74.4%,并顯著抑制肺轉(zhuǎn)移,延長(zhǎng)荷瘤小鼠生存期。腫瘤組織免疫熒光染色和流式細(xì)胞學(xué)分析進(jìn)一步驗(yàn)證了超聲輻照CPIP@EV-CM介導(dǎo)的ICD效應(yīng)以及抗腫瘤免疫激活反應(yīng)。
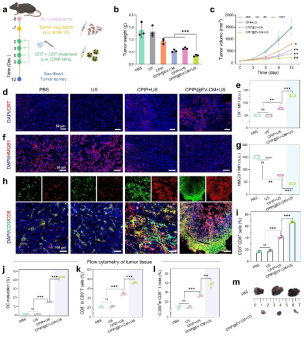
圖6. CPIP@EV-CM的體內(nèi)抗原位瘤效果
體內(nèi)小鼠肺轉(zhuǎn)移模型治療結(jié)果顯示,CPIP@EV-CM聯(lián)合超聲輻照能夠有效激活先天性和適應(yīng)性免疫應(yīng)答,有效抑制肺轉(zhuǎn)移灶形成、延長(zhǎng)荷瘤小鼠生存期。
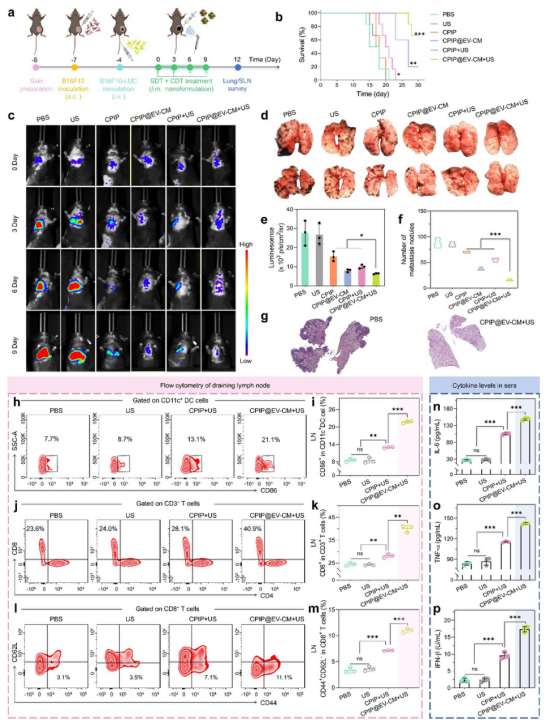
圖7. CPIP@EV-CM體內(nèi)抑制肺轉(zhuǎn)移效果評(píng)估
綜上所述,該研究通過將聲動(dòng)力/化學(xué)動(dòng)力模塊裝載于源自腫瘤細(xì)胞膜和金黃色葡萄球菌胞外囊泡膜的功能性融合膜中,設(shè)計(jì)了一種基于生物材料的納米疫苗平臺(tái)(CPIP@EV–CM)。EV–CM融合膜將腫瘤特異性抗原與天然佐劑相結(jié)合,能強(qiáng)烈刺激免疫系統(tǒng)引發(fā)抗腫瘤免疫反應(yīng)。體內(nèi)接種實(shí)驗(yàn)表明,這種融合膜能夠保護(hù)小鼠免受黑色素瘤的攻擊,凸顯了其作為預(yù)防性癌癥疫苗的潛力。在配備了 聲動(dòng)力/化學(xué)動(dòng)力模塊CPIP之后,因其既能對(duì)腫瘤細(xì)胞產(chǎn)生直接的活性氧毒性,又能增強(qiáng)免疫刺激作用,CPIP@EV–CM對(duì)已存在的腫瘤抑制效果顯著增強(qiáng)。總的來(lái)說,CPIP不僅能增強(qiáng)癌細(xì)胞的凋亡和壞死,還能誘導(dǎo)免疫原性細(xì)胞死亡以協(xié)同EV–CM的免疫刺激作用,刺激樹突狀細(xì)胞成熟和T細(xì)胞激活,在原發(fā)性和轉(zhuǎn)移性小鼠腫瘤模型中誘導(dǎo)強(qiáng)烈的抗腫瘤免疫反應(yīng)。顯然,具有不同特性(如大小和形貌)和功能(如成像、載藥)的其他輔助模塊可根據(jù)復(fù)雜需求自由選擇,這項(xiàng)工作為一類無(wú)細(xì)胞腫瘤疫苗的開發(fā)提供了一種靈活策略。
300多萬(wàn)優(yōu)質(zhì)簡(jiǎn)歷
17年行業(yè)積淀
2萬(wàn)多家合作名企業(yè)

微信掃一掃 使用小程序

