職位推薦
- 珍格醫療-臨床銷售 15001-20000
- 地奧制藥-醫藥代表 6001-8000
- 普利德醫療-醫療設備銷售經理 面議
- 大唐-兼職招商經理 面議
- 景德中藥-直營經理 6001-8000
- 安邦醫藥-省區招商經理 8001-10000
- 恒瑞醫藥-醫藥信息溝通專員 6001-8000
- 黃河中藥-學術講師 8001-10000
發布日期:2025-09-30 瀏覽次數:36
中歐夏令時間(CEST)2025年9月15至19日,第61屆歐洲糖尿病研究協會(EASD)年會在奧地利維也納舉辦。期間,恒瑞醫藥自主研發的新型長效胰島素類似物舒地胰島素(INS068)治療成人2型糖尿病(T2DM)患者的兩項關鍵III期臨床試驗(INS068-301和INS068-302)分別以簡單口頭報告形式精彩亮相。
INS068-301研究由復旦大學附屬中山醫院李小英教授作為主要研究者,帶領全國56家中心共同參與完成。INS068-302研究由北京大學人民醫院紀立農教授作為主要研究者,帶領全國68家中心共同參與完成。兩項研究結果表明,在口服降糖藥控制不佳或基礎胰島素控制不佳的T2DM患者中,舒地胰島素在血糖控制方面顯示出與甘精胰島素相當的療效,且夜間低血糖風險明顯降低[1]。本文詳細介紹兩項關鍵III期臨床試驗的研究設計、研究結果及在T2DM人群中的潛在應用前景。

2025 EASD現場圖:
北京大學人民醫院高蕾莉教授就INS068-302研究做口頭報告

2025 EASD現場圖:
恒瑞醫藥陳虹博士就INS068-301研究做口頭報告
研究背景和目的
T2DM是?種慢性進展性疾病,隨著病程發展,常需要聯合兩種或兩種以上降糖藥物以維持血糖控制。基礎胰島素是T2DM治療的重要手段,但低血糖風險,尤其是夜間低血糖,是其臨床應用中的主要挑戰。
舒地胰島素是?種新型的可溶性長效胰島素類似物,每日?次皮下注射給藥。藥物半衰期約為21小時,在穩態下正葡萄糖鉗夾試驗中降糖效果可持續超過42小時[2]。
INS068-301與INS068-302為兩項隨機、開放標簽、平行對照設計的III期臨床研究,分別納入基礎胰島素經治后血糖控制不佳以及口服降糖藥經治后血糖控制不佳的T2DM患者,進行舒地胰島素與甘精胰島素的頭對頭對比。兩項研究的目的為評估舒地胰島素在中國T2DM患者中的療效與安全性,本報告對兩項研究的關鍵數據進行匯總呈現。
INS068-301研究:舒地胰島素(INS068)與甘精胰島素在基礎胰島素控制不佳的T2DM患者中的療效和安全性比較
01研究設計
研究納入已接受基礎胰島素治療≥8周,糖化血紅蛋白(HbA1c)7.0%-10.0%的成年T2DM患者。符合納入標準的受試者按1:1比例隨機分組,接受INS068或甘精胰島素(IGlar)每日一次(QD)皮下注射治療。胰島素起始劑量根據患者此前使用的基礎胰島素劑量進行換算,治療期間進行劑量滴定(目標血糖:早餐前自我監測指尖血糖 3.9~5.6mmol/L)。
本研究的主要終點指標為治療第26周HbA1c相對基線變化,采用非劣效性檢驗進行統計分析,設定非劣效界值為0.4%。

圖1:INS068-301研究設計(ClinicalTrials.gov, NCT05702073)
02研究結果
1基線特征
研究共入組423例中國成人T2DM受試者,INS068組和IGlar組分別入組211例和212例。
兩組受試者人口學和其他基線特征相似,具有可比性。INS068組和IGlar組中,平均年齡分別為58.3歲和58.5歲,男性占比分別為62.1%和55.7%,平均BMI分別為24.78 kg/m2和24.83 kg/m2,平均HbA1c分別為8.30%和8.36%,平均空腹血糖(FPG)分別為8.34 mmol/L和8.51 mmol/L,基礎胰島素的平均日劑量分別為16.1 U和16.6 U。

表1:INS068-301研究基線特征
2降糖療效
本研究達到預設的主要終點,治療26周后,INS068組的HbA1c相對基線變化非劣于IGlar組。INS068組與IGlar組的HbA1c降幅分別為0.70%和0.83%,兩組差值為 0.13%(95% CI:-0.05,0.31)。

圖2:INS068-301研究主要終點:治療第26周HbA1c相對基線變化
治療26周后,INS068組FPG降幅大于IGlar組(均值變化:-2.40 mmol/L vs -1.96 mmol/L;兩組差值:-0.45 mmol/L,95% CI:-0.74,-0.16)。

圖3:INS068-301次要終點:26周時FPG較基線的變化
兩組受試者在接受治療12周后,早餐前自我監測血糖(SMPG)趨于穩定,且兩組各訪視前三天的早餐前SMPG均值基本一致。治療第26周,INS068組與IGlar組的每日胰島素劑量分別為 0.46 U/kg和0.48 U/kg。
3安全性
研究期間,INS068組和IGlar組治療期間出現的不良事件(AE)和治療相關AE的發生率均相當。INS068組和IGlar組的SAE發生率相當,且均與治療無關。研究期間未發生導致治療提前終止、暫停用藥的AE。
與IGlar組相比,INS068組的總低血糖發生率在數值上低于IGlar組(兩組發生率分別為48.6% vs 53.8%,風險比0.90 [0.75, 1.09]),且夜間總低血糖風險低于IGlar組(兩組發生率分別為21.9% vs 33.5%,風險比0.65 [0.48, 0.90])。
INS068-302研究:舒地胰島素(INS068)與甘精胰島素在口服降糖藥控制不佳的T2DM患者中的療效及安全性比較
01研究設計
研究納入已接受穩定劑量口服降糖藥(OADs)治療≥8周,HbA1c 7.0%-11.0%的成年T2DM患者。符合納入標準的患者按2:1比例隨機分組,分別接受INS068或IGlar每日一次(QD)皮下注射治療。胰島素起始劑量為每日10 U,治療期間進行劑量滴定(目標血糖:早餐前自我監測指尖血糖3.9~5.6 mmol/L)。
研究的主要終點指標為治療第26周HbA1c相對基線變化,采用非劣效性檢驗進行統計分析,設定非劣效界值為0.4%。

圖4:INS068-302研究設計(ClinicalTrials.gov, NCT05699408)
02研究結果
1基線特征
研究共入組513例中國成人T2DM受試者,INS068組和IGlar組分別入組341例和172例。
兩組受試者人口學和其他基線特征相似,具有可比性。INS068組和IGlar組中,平均年齡分別為56.7歲和55.7歲,男性占比分別為60.1%和64.0%,平均BMI分別為24.9kg/m2和25.0 kg/m2,平均HbA1c分別為8.44%和8.47%,FPG分別為9.32 mmol/L和9.36 mmol/L。

表2:INS068-302研究基線特征
2降糖療效
本研究達到預設的主要終點,治療26周后,INS068組的HbA1c相對基線變化非劣于IGlar組。INS068 組與 IGlar組的HbA1c降幅分別為 1.34% 和 1.36%, 兩組差值為 0.02%(95% CI:-0.14%,0.18%)。
治療26周后,兩組FPG降幅相當(分別為 3.35 mmol/L vs 3.21 mmol/L)。
兩組降糖效果均可維持至治療第52周,且組間療效相當。
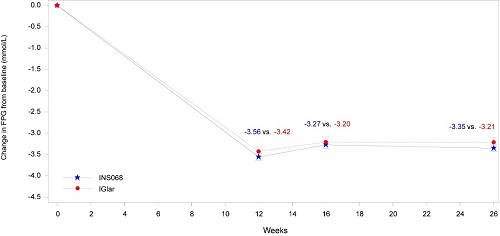
圖5:INS068-302研究主要終點:HbA1c較基線的變化

圖6:INS068-302研究次要終點:FPG較基線的變化
兩組受試者在治療8周左右,早餐前SMPG趨于穩定,且兩組各訪視前三天的早餐前SMPG均值基本一致。治療第26周,INS068組和IGlar組每日胰島素劑量分別為0.36 U/kg和0.38 U/kg;治療第52周,兩組胰島素劑量分別滴定調整為0.38 U/kg和0.40 U/kg。
3安全性
本研究INS068組和IGlar組治療期間出現的AE、治療相關AE和SAE的發生率相當。
在26周治療期間,INS068組的總低血糖發生率與夜間總低血糖發生率數值低于IGlar組(兩組總低血糖發生率分別為34.7% vs 41.3%,風險比0.84 [0.67, 1.06];兩組夜間總低血糖發生率分別為14.5% vs 18.6%,風險比0.78 [0.52, 1.17])。
在52周治療期間,INS068組的總低血糖風險與夜間總低血糖風險均明顯低于IGlar組(兩組總低血糖發生率分別為43.6% vs 54.7%,風險比0.80 [0.67, 0.96];兩組夜間總低血糖發生率分別為19.6% vs 30.2%,風險比0.65 [0.47, 0.89])。
研究結論
INS068-301和INS068-302兩項關鍵性III期臨床研究的結果表明,在兩種不同治療背景(基礎胰島素控制不佳或?服降糖藥控制不佳)的中國T2DM患者中,相較于甘精胰島素,舒地胰島素(INS068)可在控糖同時降低低血糖風險,有望為2型糖尿病患者提供?種全新的治療選擇。
參考文獻:
[1] https://www.easd.org/annual-meeting/easd-2025/programme/
[2] Hompesch M, et al. Pharmacodynamics, Pharmacokinetics, Safety, and Tolerability of INS068 vs Insulin Degludec in Type 1 Diabetes at Steady State: a Phase I, Randomised, Double-blind, Cross-over Trial. the 57th Annual Meeting of EASD, 27 Sep~ 1 Oct. 2021, Stockholm Sweden, Abstract OP 36.
聲明:
1.本新聞旨在分享學術前沿動態,僅供醫療衛生專業人士基于學術目的參閱,非廣告用途。
2.恒瑞醫藥不推薦任何未被批準的藥品、適應癥的使用。
300多萬優質簡歷
17年行業積淀
2萬多家合作名企業

微信掃一掃 使用小程序

